Здравствуйте, уважаемые химики!
Для научного электрофизиологического эксперимента нужно получить свободные ионы Ag2+ в водном растворе. Какое соединение нужно взять? Подойдет ли для этой цели пиколинат серебра? Не будут ли ионы Ag2+ взаимодействовать с ионами Cl- (водный раствор в стандартных усиловиях содержит KCl, но его можно заменить на KGluconate если необходимо отсутствие ионов Cl-).
Что посоветуете? Спасибо всем, кто сможет помочь.
Ионы Ag2+ в водном растворе - реально ли?
Ионы Ag2+ в водном растворе - реально ли?
Последний раз редактировалось dess 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
Последний раз редактировалось Таланов 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
Правильно, значит надо будет взять
Последний раз редактировалось dess 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
А как насчет дистиллированной воды? Дорого? Растворить в ней 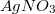 ... Я тоже не химик...
... Я тоже не химик...
Последний раз редактировалось grigoriy 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
Все соли в аналитической химии по умолчанию растворены в дистилляте.
А кто, ещё?
dess писал(а):Source of the post
Я не силен в химии, но мне кажется остальные вещества, которые содержат, будут реагировать с водой.
Что значит реагировать с водой? Образовывать новые соединения? Карбид кальция например реагирует с водой, металлический литий, натрий, калий, железо и т.д.
Последний раз редактировалось Таланов 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
Таланов писал(а):Source of the postdess писал(а):Source of the post
Я не силен в химии, но мне кажется остальные вещества, которые содержат, будут реагировать с водой.
Что значит реагировать с водой? Образовывать новые соединения? Карбид кальция например реагирует с водой, металлический литий, натрий, калий, железо и т.д.
Сайт
Последний раз редактировалось balans 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
grigoriy писал(а):Source of the post
А как насчет дистиллированной воды? Дорого? Растворить в ней... Я тоже не химик...
В водном растворе
Последний раз редактировалось dess 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
нужно получить свободные ионы Ag2+ в водном растворе
Двухвалентное серебро в водном растворе разлагается, окисляя воду до кислорода.
Последний раз редактировалось Jeffry 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
Jeffry писал(а):Source of the post
Двухвалентное серебро в водном растворе разлагается, окисляя воду до кислорода.
Вот, это именно то, что я хотел узнать. Спасибо!
Получается, что ряд металлов расширить не получится.
Последний раз редактировалось dess 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Ионы Ag2+ в водном растворе - реально ли?
Аg2+ обязательно окислит Cl-, а уже потом Аg+ свяжется с хлорид-ионом.
Последний раз редактировалось Alex 94 28 ноя 2019, 06:57, всего редактировалось 1 раз.
Причина: test
Причина: test
Кто сейчас на форуме
Количество пользователей, которые сейчас просматривают этот форум: нет зарегистрированных пользователей и 7 гостей