О гипотезах Дальтона и числе Авогадро.
Добавлено: 11 апр 2015, 10:51
О ГИПОТЕЗАХ ДАЛЬТОНА И ЧИСЛЕ АВОГАДРО
Фёдоров В.В., Пономарёв Д.А., Бондаренко Т.В.
Запишем уравнение химической реакции между элементами X и Y в таком виде:
 (1)
(1)
где X, Y – символ химического элемента с некоторой атомной массой, A, B – соответственно число атомов элемента, вступающего в реакцию, C – число бинарных молекул, получающихся в результате реакции, k, n – стехиометрические коэффициенты бинарного химического соединения.
Уравнение (1) есть не что иное, как запись закона сохранения массы с использованием величин атомной массы химических элементов и их количества, то есть
 (2)
(2)
где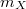 – масса элемента X,
– масса элемента X, 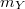 – масса элемента Y, а
– масса элемента Y, а 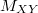 – масса химического соединения.
– масса химического соединения.
Поскольку , а
, а  (A, B, C, k, n – целые числа), то
(A, B, C, k, n – целые числа), то
 (3)
(3)
Разделим одно на другое и получим
 . (4)
. (4)
Соотношение (4) является исходным в решении одной из основных проблем всего естествознания – проблемы структурной организации материи на атомно-молекулярном уровне. Кроме того, оно определяет и строгую последовательность её поэтапного решения: первый – строение и состав атомов стабильных химических элементов, второй – строение и состав молекул бинарных химических соединений. Качественное решение этой неразрывной совокупности проблем, несомненно, не может быть получено с использованием физически полуосмысленных гипотез.
Действительно, в конечном виде соотношение (4) связывает между собой всего шесть количественных характеристик химической реакции (1), притом только две определяются экспериментально, а их отношение не зависит от C. Следовательно, неизвестная С, именуемая числом Авогадро, автоматичеcки исключается, что и соответствует её роли не только в атомно-молекулярном учении, но и во всём теоретическом естествознании.
Если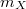 и
и 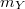 определяются экспериментально, то в соотношении (4) остаются четыре неизвестные, которые в принципе не могут принимать произвольных значений, так как это соотношение является исходным указателем пути для решения проблемы определения атомных масс стабильных химических элементов. Иного пути просто не существует, а гипотезы, которые не согласуются с фундаментальными законами первичных центрально-потенциальных природных взаимодействий, вряд ли способствуют созданию теоретически обоснованных моделей строения и состава атомов стабильных элементов и устойчивых молекул. (Речь не идёт о бессмысленных законах Ньютона и Кулона.)
определяются экспериментально, то в соотношении (4) остаются четыре неизвестные, которые в принципе не могут принимать произвольных значений, так как это соотношение является исходным указателем пути для решения проблемы определения атомных масс стабильных химических элементов. Иного пути просто не существует, а гипотезы, которые не согласуются с фундаментальными законами первичных центрально-потенциальных природных взаимодействий, вряд ли способствуют созданию теоретически обоснованных моделей строения и состава атомов стабильных элементов и устойчивых молекул. (Речь не идёт о бессмысленных законах Ньютона и Кулона.)
Дальтон, пожалуй, и не осознавал всей сложности решения указанной проблемы и важности для человеческой практики в будущем, а поэтому и избрал гипотетический путь её решения, а именно:
а) Признавая, что масса атомов химических элементов чрезвычайно мала и определить её непосредственным взвешиванием не удастся, Дальтон предложил определять относительные величины атомных масс элементов, принимая массу атома водорода, как самого лёгкого, за единицу. В этом случае в соотношении (4) число неизвестных сокращается до трёх, что ещё не приводит к решению поставленной задачи;
б) Если бы водород, выбранный в качестве стандарта атомной массы, вступал в химические реакции со всеми остальными и образовывал бинарные химические соединения с одним и тем же атомным (ионным) составом, то задача определения относительных величин атомных масс элементов была бы решена сразу с использованием соотношения (4). На практике этого не наблюдается. Многие элементы, соединяясь друг с другом при различных внешних условиях, образуют два и более соединения. Этот факт свидетельствует о том, что без определения стехиометрических коэффициентов бинарных химических соединений решить проблему определения величин относительных атомных масс элементов нельзя. Дальтон и из этого тупика находит выход. Он выдвигает дополнительную гипотезу о составе молекул бинарных химических соединений, то есть постулирует таблицу стехиометрических коэффициентов.
Вот таким образом соотношение (4), являясь количественным отражением закона сохранения массы с четырьмя неизвестными, было превращено в уравнение с одним неизвестным, решить которое особого труда не составляет, но надеяться, что такие “теоретические вольности” могут привести к положительным результатам в познании реального строения и состава атомов и молекул, не приходится.
Действительно, безобидное на первый взгляд предложение Дальтона определять относительные величины атомных масс элементов (X/Y) сегодня означает не что иное, как отказ от понятия атома с присущими индивидуальными свойствами и способностью к самостоятельному существованию в пространстве в качестве элементарной трёхмерной структуры материи. Добавим к этому ещё и дальтоновский произвол стехиометрического состава молекул бинарных химических соединений, который даже не согласован с трёхмерным строением молекул, то получаем удручающий перечень исходных данных для систематизации химических элементов в периодическую систему. Например, о каком теоретическом обосновании гипотезы Дальтона о составе молекул бинарных химических соединений может идти речь, если в ней не учитываются даже всем известные ещё со школьной скамьи положения: два или три центра взаимодействия атомов (ионов) химических элементов не могут образовывать устойчивой трёхмерной молекулы. (Даже математическое трёхмерное пространство обозначено четырьмя точками.) Перечень стехиометрических коэффициентов Дальтона в принципе противоречит реальности, а поэтому величины атомных масс всех ныне известных стабильных химических элементов, отражённые в современной периодической систематике, ошибочны.
Следует отметить, что бесплодные гипотезы Дальтона были признаны его современниками и многочисленной армией последователей до наших дней в качестве достоверных и задержали развитие науки в области так называемого микромира (теоретическую химию и физику микромира) минимум на столетие, постепенно дополняя соответствующими и загоняя её в безнадежный тупик.
К последователям Дальтона относится Д. И. Менделеев, который систематизировал известные в то время химические элементы по мнимым величинам их относительных атомных масс под вымышленный периодический закон. Бессмысленно заниматься систематизацией того, что ничего общего не имеет с реальностью. Периодичности в этом законе нет, а видимость её уже столетие пытаются обосновать с использованием таких же по смыслу и значению гипотез, как и гипотезы Дальтона. Утверждение Менделеева (1905 г.): “По-видимому, периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещается”, – уже в то время надо было воспринимать с точностью до наоборот, так как это не закон природы, а какое-то недоразумение. В таких законах теоретическое естествознание не нуждается.
“Авогадро постоянная (число Авогадро) – число структурных элементов (атомов, молекул, ионов или др. ч-ц) в ед. кол-ва в-ва (в одном моле). … Авогадро постоянная – одна из фундаментальных физических констант, существенная для определения мн. других физ. констант (Больцмана постоянная, Фарадея постоянная и др.). Один из лучших эксперим. методов определения А. п. основан на измерениях электрич. заряда, необходимого для электролитич. разложения известного числа молей сложного в-ва и заряда эл-на. Наиболее достоверное значение А. п. (на 1980)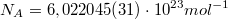 ” [1, стр.8]. “Моль – количество в-ва, содержащее столько же структурных элементов, сколько содержится атомов в 0,012 кг
” [1, стр.8]. “Моль – количество в-ва, содержащее столько же структурных элементов, сколько содержится атомов в 0,012 кг 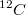 . Структурные элементы м.б. атомами, молекулами, ионами, электронами и др. частицами, в т. ч. условными ...” [2, стр. 351].
. Структурные элементы м.б. атомами, молекулами, ионами, электронами и др. частицами, в т. ч. условными ...” [2, стр. 351].
Сразу отметим, что в настоящее время гипотезу Авогадро считают даже законом, так как она якобы проверена на обширном опытном материале. Изложенный выше пример с выполнением закона сохранения массы в химической реакции между двумя элементами доказывает (см. результат в виде соотношения (4)), что о каком-либо значении для теоретического естествознания не только самого числа Авогадро, но и классических понятий грамм-атом и грамм-молекула не может быть и речи. Эти число и понятия привнесены в классику по недоразумению, что однозначно и подтверждает соотношение (4).
Действительно, взвесить отдельный атом или отдельную молекулу явно невозможно, а значит и непосредственно сосчитать число атомов или молекул, например, в газе определённых объёма и внешних условий так же невозможно даже в том случае, если известна его общая масса. Этим сразу ставится под сомнение сама целесообразность постулата о существовании постоянной Авогадро в теоретическом естествознании. Это подтверждает и следствие из закона сохранения массы, записанное в виде соотношения (4) с использованием символов атомных масс элементов и неизвестных количеств атомов (ионов) элементов в составе молекул бинарного химического соединения. Это во-первых, а во-вторых, объективность результатов экспериментов по определению соотношений масс элементов, которые не зависят от массы при разложении бинарных химических соединений состава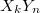 – любое целое число от единицы и далее в зависимости
– любое целое число от единицы и далее в зависимости 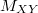 , заявляет, что соотношение (4) приобретает свою значимость только в совокупности с разработкой теорий состава и строения атомов и молекул, которые освобождены от спекулятивных догм классики.
, заявляет, что соотношение (4) приобретает свою значимость только в совокупности с разработкой теорий состава и строения атомов и молекул, которые освобождены от спекулятивных догм классики.
Итак, все постоянные современного классического теоретического естествознания, связанные с постоянной Авогадро (например, постоянная Фарадея, молярная газовая постоянная, объём моля идеального газа при нормальных условиях, постоянная Больцмана [1]), следует считать ошибочными. Этим ошибкам нет места в теоретическом естествознании ХХI-го столетия.
Литература
1. Физический энциклопедический словарь. М., “Советская энциклопедия”, 1983.
2. Химический энциклопедический словарь. М., “Советская энциклопедия”, 1983.
С уважением, авторы.
Фёдоров В.В., Пономарёв Д.А., Бондаренко Т.В.
Запишем уравнение химической реакции между элементами X и Y в таком виде:
где X, Y – символ химического элемента с некоторой атомной массой, A, B – соответственно число атомов элемента, вступающего в реакцию, C – число бинарных молекул, получающихся в результате реакции, k, n – стехиометрические коэффициенты бинарного химического соединения.
Уравнение (1) есть не что иное, как запись закона сохранения массы с использованием величин атомной массы химических элементов и их количества, то есть
где
Поскольку
Разделим одно на другое и получим
Соотношение (4) является исходным в решении одной из основных проблем всего естествознания – проблемы структурной организации материи на атомно-молекулярном уровне. Кроме того, оно определяет и строгую последовательность её поэтапного решения: первый – строение и состав атомов стабильных химических элементов, второй – строение и состав молекул бинарных химических соединений. Качественное решение этой неразрывной совокупности проблем, несомненно, не может быть получено с использованием физически полуосмысленных гипотез.
Действительно, в конечном виде соотношение (4) связывает между собой всего шесть количественных характеристик химической реакции (1), притом только две определяются экспериментально, а их отношение не зависит от C. Следовательно, неизвестная С, именуемая числом Авогадро, автоматичеcки исключается, что и соответствует её роли не только в атомно-молекулярном учении, но и во всём теоретическом естествознании.
Если
Дальтон, пожалуй, и не осознавал всей сложности решения указанной проблемы и важности для человеческой практики в будущем, а поэтому и избрал гипотетический путь её решения, а именно:
а) Признавая, что масса атомов химических элементов чрезвычайно мала и определить её непосредственным взвешиванием не удастся, Дальтон предложил определять относительные величины атомных масс элементов, принимая массу атома водорода, как самого лёгкого, за единицу. В этом случае в соотношении (4) число неизвестных сокращается до трёх, что ещё не приводит к решению поставленной задачи;
б) Если бы водород, выбранный в качестве стандарта атомной массы, вступал в химические реакции со всеми остальными и образовывал бинарные химические соединения с одним и тем же атомным (ионным) составом, то задача определения относительных величин атомных масс элементов была бы решена сразу с использованием соотношения (4). На практике этого не наблюдается. Многие элементы, соединяясь друг с другом при различных внешних условиях, образуют два и более соединения. Этот факт свидетельствует о том, что без определения стехиометрических коэффициентов бинарных химических соединений решить проблему определения величин относительных атомных масс элементов нельзя. Дальтон и из этого тупика находит выход. Он выдвигает дополнительную гипотезу о составе молекул бинарных химических соединений, то есть постулирует таблицу стехиометрических коэффициентов.
Вот таким образом соотношение (4), являясь количественным отражением закона сохранения массы с четырьмя неизвестными, было превращено в уравнение с одним неизвестным, решить которое особого труда не составляет, но надеяться, что такие “теоретические вольности” могут привести к положительным результатам в познании реального строения и состава атомов и молекул, не приходится.
Действительно, безобидное на первый взгляд предложение Дальтона определять относительные величины атомных масс элементов (X/Y) сегодня означает не что иное, как отказ от понятия атома с присущими индивидуальными свойствами и способностью к самостоятельному существованию в пространстве в качестве элементарной трёхмерной структуры материи. Добавим к этому ещё и дальтоновский произвол стехиометрического состава молекул бинарных химических соединений, который даже не согласован с трёхмерным строением молекул, то получаем удручающий перечень исходных данных для систематизации химических элементов в периодическую систему. Например, о каком теоретическом обосновании гипотезы Дальтона о составе молекул бинарных химических соединений может идти речь, если в ней не учитываются даже всем известные ещё со школьной скамьи положения: два или три центра взаимодействия атомов (ионов) химических элементов не могут образовывать устойчивой трёхмерной молекулы. (Даже математическое трёхмерное пространство обозначено четырьмя точками.) Перечень стехиометрических коэффициентов Дальтона в принципе противоречит реальности, а поэтому величины атомных масс всех ныне известных стабильных химических элементов, отражённые в современной периодической систематике, ошибочны.
Следует отметить, что бесплодные гипотезы Дальтона были признаны его современниками и многочисленной армией последователей до наших дней в качестве достоверных и задержали развитие науки в области так называемого микромира (теоретическую химию и физику микромира) минимум на столетие, постепенно дополняя соответствующими и загоняя её в безнадежный тупик.
К последователям Дальтона относится Д. И. Менделеев, который систематизировал известные в то время химические элементы по мнимым величинам их относительных атомных масс под вымышленный периодический закон. Бессмысленно заниматься систематизацией того, что ничего общего не имеет с реальностью. Периодичности в этом законе нет, а видимость её уже столетие пытаются обосновать с использованием таких же по смыслу и значению гипотез, как и гипотезы Дальтона. Утверждение Менделеева (1905 г.): “По-видимому, периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещается”, – уже в то время надо было воспринимать с точностью до наоборот, так как это не закон природы, а какое-то недоразумение. В таких законах теоретическое естествознание не нуждается.
“Авогадро постоянная (число Авогадро) – число структурных элементов (атомов, молекул, ионов или др. ч-ц) в ед. кол-ва в-ва (в одном моле). … Авогадро постоянная – одна из фундаментальных физических констант, существенная для определения мн. других физ. констант (Больцмана постоянная, Фарадея постоянная и др.). Один из лучших эксперим. методов определения А. п. основан на измерениях электрич. заряда, необходимого для электролитич. разложения известного числа молей сложного в-ва и заряда эл-на. Наиболее достоверное значение А. п. (на 1980)
Сразу отметим, что в настоящее время гипотезу Авогадро считают даже законом, так как она якобы проверена на обширном опытном материале. Изложенный выше пример с выполнением закона сохранения массы в химической реакции между двумя элементами доказывает (см. результат в виде соотношения (4)), что о каком-либо значении для теоретического естествознания не только самого числа Авогадро, но и классических понятий грамм-атом и грамм-молекула не может быть и речи. Эти число и понятия привнесены в классику по недоразумению, что однозначно и подтверждает соотношение (4).
Действительно, взвесить отдельный атом или отдельную молекулу явно невозможно, а значит и непосредственно сосчитать число атомов или молекул, например, в газе определённых объёма и внешних условий так же невозможно даже в том случае, если известна его общая масса. Этим сразу ставится под сомнение сама целесообразность постулата о существовании постоянной Авогадро в теоретическом естествознании. Это подтверждает и следствие из закона сохранения массы, записанное в виде соотношения (4) с использованием символов атомных масс элементов и неизвестных количеств атомов (ионов) элементов в составе молекул бинарного химического соединения. Это во-первых, а во-вторых, объективность результатов экспериментов по определению соотношений масс элементов, которые не зависят от массы при разложении бинарных химических соединений состава
Итак, все постоянные современного классического теоретического естествознания, связанные с постоянной Авогадро (например, постоянная Фарадея, молярная газовая постоянная, объём моля идеального газа при нормальных условиях, постоянная Больцмана [1]), следует считать ошибочными. Этим ошибкам нет места в теоретическом естествознании ХХI-го столетия.
Литература
1. Физический энциклопедический словарь. М., “Советская энциклопедия”, 1983.
2. Химический энциклопедический словарь. М., “Советская энциклопедия”, 1983.
С уважением, авторы.