Задачи по аналитике
Добавлено: 13 апр 2013, 15:08
Проверьте, пожалуйста, решения задач:
1)Обнаруживаемый минимум реакци иона кальция с аммония оксалатом равен 0,15мкг при минимальном объёме предельно разбавленного раствора 0,01 мл. Определите предельное разбавление для данной реакции и предельную концентрацию.
Ca2++C2O42-=CaC2O4
m=(Vmin/Vlim)*106
Vlim=(Vmin/m)*106=(0,05мл/0,15мкг)*106=3*105мл/г
Clim=1/Vlim=1/3*105=3*10-4г/мл
2)Какой осадок выпадет первым, если к раствору, содержащему 0,01моль бария нитрата и 0,02 моль кальция нитрата прибавить избыток раствора серной кислоты.
BaNO3+CaNO3+2H2SO4изб=BaSO4+CaSO4+2H2NO3
BaSO4=Ba2++SO42-
CaSO4=Ca2++SO42-
Ks=[Ba2+]*[SO42-]=1,1*10-10
Ks=[Ca2+]*[SO42-]=2,5*10-5
[SO4]=Ks/[BaNO3]=1,1*10-10/0,01моль=110*10-10моль/л
[SO4]=Ks/[CaNO3]=2,5*10-5/0,02моль=125*10-5моль/л
125*10-5>110*10-10 CaSO4 выпадает первым в осадок
3)Приведите уравнение реакции гидролиза, рассчитайте константу гидролиза, степень гидролиза и рН 0,01 моль/л раствора алюминия нитрата.
Кг=KH2O/Ko=1/1,38*10-9=7,246*10-6
[H+]=
рН=-lg[H+]=lg2,7*lg10-4=0,413+(-4)=-3,587
pH=3,587
[H+=$$\sqrt{Êã*Ñî} -4 h=$$" title="$$=2,7*10-4 h=$$" align="middle" style="border: 0; vertical-align: middle">\sqrt{Kã/Ñ}
-4 h=$$" title="$$=2,7*10-4 h=$$" align="middle" style="border: 0; vertical-align: middle">\sqrt{Kã/Ñ}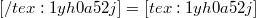 $$" title="$$=$$" align="middle" style="border: 0; vertical-align: middle">\sqrt{2,7*10^-2}$$=1,7*10-
$$" title="$$=$$" align="middle" style="border: 0; vertical-align: middle">\sqrt{2,7*10^-2}$$=1,7*10-
1)Обнаруживаемый минимум реакци иона кальция с аммония оксалатом равен 0,15мкг при минимальном объёме предельно разбавленного раствора 0,01 мл. Определите предельное разбавление для данной реакции и предельную концентрацию.
Ca2++C2O42-=CaC2O4
m=(Vmin/Vlim)*106
Vlim=(Vmin/m)*106=(0,05мл/0,15мкг)*106=3*105мл/г
Clim=1/Vlim=1/3*105=3*10-4г/мл
2)Какой осадок выпадет первым, если к раствору, содержащему 0,01моль бария нитрата и 0,02 моль кальция нитрата прибавить избыток раствора серной кислоты.
BaNO3+CaNO3+2H2SO4изб=BaSO4+CaSO4+2H2NO3
BaSO4=Ba2++SO42-
CaSO4=Ca2++SO42-
Ks=[Ba2+]*[SO42-]=1,1*10-10
Ks=[Ca2+]*[SO42-]=2,5*10-5
[SO4]=Ks/[BaNO3]=1,1*10-10/0,01моль=110*10-10моль/л
[SO4]=Ks/[CaNO3]=2,5*10-5/0,02моль=125*10-5моль/л
125*10-5>110*10-10 CaSO4 выпадает первым в осадок
3)Приведите уравнение реакции гидролиза, рассчитайте константу гидролиза, степень гидролиза и рН 0,01 моль/л раствора алюминия нитрата.
Кг=KH2O/Ko=1/1,38*10-9=7,246*10-6
[H+]=
рН=-lg[H+]=lg2,7*lg10-4=0,413+(-4)=-3,587
pH=3,587
[H+=$$\sqrt{Êã*Ñî}