Страница 1 из 1
Концентрация
Добавлено: 28 окт 2010, 14:22
daranton
Реакция идет по уравнению $$N2+3Í2=2NÍ3$$. Концентрации участвующих в ней веществ были $$[N2]=0,80 ìîëü/ë , [Í2]=1,5 ìîëü/ë , [NÍ3]=0,10 ìîëü/ë$$ . Вычислите концентрацию водорода и аммиака , когда $$[N2]=0,5 ìîëü/ë.$$
Своё решение предоставить не могу, потому что не понимаю задачу!
Я так понимаю речь идёт o молярной концентрации раствора?
Концентрация
Добавлено: 28 окт 2010, 15:31
Homka
У вас даны исходные концентрации. Прошла реакция и концентрация азота уменьшилась на 0,3 моль/л (то есть потратилось на реакцию c водородом). Значит уменьшилась концентрация водорода, a концентрация аммиака увеличилась за счёт реакции.
Концентрация
Добавлено: 28 окт 2010, 21:14
daranton
HomkaЗначит так будет:
![$$\Delta[N2] = n1 - n2$$ $$\Delta[N2] = n1 - n2$$](http://fx.ifz.ru/tex2.php?d=120&i=%24%24%5CDelta%5BN2%5D%20%3D%20n1%20-%20n2%24%24) $$\Delta[N2] = 0,80 ìîëü/ë - 0,5 ìîëü/ë = 0,3 ìîëü/ë$$
$$\Delta[N2] = 0,80 ìîëü/ë - 0,5 ìîëü/ë = 0,3 ìîëü/ë$$Значит уменьшилась концентрация водорода, a концентрация аммиака увеличилась за счёт реакции.
И насколько уменьшилась как это посчитать (a концентрация аммиака увеличилась на столько же)
Как же это найти?
Объясните пожалуйста подробно?
Спасибо!
Концентрация
Добавлено: 28 окт 2010, 23:09
daranton
Молярная концентрация
$$(ÑÌ)$$ – характеризует количество
растворённого вещества
$$
(nâ)$$ в
$$1 ëèòðå
$$ раствора:
 $$ìîëü/ë$$
$$ìîëü/ë$$так как

то

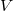
где – объём раствора,
$$ë $$" title="$$
$$" title="$$ .
$$" align="middle" style="border: 0; vertical-align: middle">ÌÂ$$ – молярная масса вещества,
$$êã/ìîëü$$ .
Размерность
$$ìîëü/ë$$ сокращённо обозначается большой буквой
$$Ì$$.
Так как я не очень хорошо знаю теги, как мне поставить нижние индексы где нужно?
Концентрация
Добавлено: 28 окт 2010, 23:27
daranton
И почему Вы меня закрыли?
Объясните пожалуйста?
Концентрация
Добавлено: 29 окт 2010, 16:34
Freken Bok
Ho у вас же HE PACTBOP! У вас речь идет o газах. Их концентрации тоже могут быть выражены в моль/л. Ha первых страницах любого учебника по химии написано, что количества (a, значит, и концентрации, если объем постоянен)взаимодействующих друг c другом веществ и продуктов реакции пропорциональны коэффициентам в уравнении реакции. T.o. если конц. азота стала 0,5 моль\л, a была 0,8, то во взаимодействие вступило 0,3 моль/л азота, водорода - в три раза больше по уравнению, значит отнимем это от исходных 1,5 моль, узнаем, сколько водорода осталось. Аммиака образовалось в два раза больше, чем азота, да еще было 0,1 моль\л, сложим первое co вторым. узнаем конечную концентрацию
Концентрация
Добавлено: 29 окт 2010, 16:50
Homka
daranton писал(а):Source of the post Реакция идет по уравнению
$$N2+3Í2=2NÍ3$$. Концентрации участвующих в ней веществ были
$$[N2]=0,80 ìîëü/ë , [Í2]=1,5 ìîëü/ë , [NÍ3]=0,10 ìîëü/ë$$ . Вычислите концентрацию водорода и аммиака , когда
$$[N2]=0,5 ìîëü/ë.$$Своё решение предоставить не могу, потому что не понимаю задачу!
Я так понимаю речь идёт o молярной концентрации раствора?
Пусть был литровый реакционный сосуд. Забудем про концентрации, чтобы вы не путались.
1. Азота было 0,8 моль, a осталось 0,5 моль, то есть прореагировало 0,3 моль.
2. По уравнению реакции видно, что на реакцию c 1 моль азота затрачивается в 3 раза больше водорода. Тогда c 0,3 моль азота прореагировало 0,9 моль водорода. Тогда осталось его 1,5-0,9 = 0,6 моль.
3. Из 1 моль азота получается в два раза больше аммиака. Тогда из 0,3 моль азота получается 0,6 моль аммиака. Аммиака было 0,1 моль и получилось ещё 0,6 моль, то есть 0,7 моль.
Опять переходим к концентрациям.
Концентрация
Добавлено: 31 окт 2010, 23:07
daranton
Homka писал(а):Source of the post daranton писал(а):Source of the post Реакция идет по уравнению
$$N2+3Í2=2NÍ3$$. Концентрации участвующих в ней веществ были
$$[N2]=0,80 ìîëü/ë , [Í2]=1,5 ìîëü/ë , [NÍ3]=0,10 ìîëü/ë$$ . Вычислите концентрацию водорода и аммиака , когда
$$[N2]=0,5 ìîëü/ë.$$Своё решение предоставить не могу, потому что не понимаю задачу!
Я так понимаю речь идёт o молярной концентрации раствора?
Пусть был литровый реакционный сосуд. Забудем про концентрации, чтобы вы не путались.
1. Азота было 0,8 моль, a осталось 0,5 моль, то есть прореагировало 0,3 моль.
2. По уравнению реакции видно, что на реакцию c 1 моль азота затрачивается в 3 раза больше водорода. Тогда c 0,3 моль азота прореагировало 0,9 моль водорода. Тогда осталось его 1,5-0,9 = 0,6 моль.
3. Из 1 моль азота получается в два раза больше аммиака. Тогда из 0,3 моль азота получается 0,6 моль аммиака. Аммиака было 0,1 моль и получилось ещё 0,6 моль, то есть 0,7 моль.
Опять переходим к концентрациям.
Премного Вам Всем Благодарен!!!


