Arwen писал(а):Source of the post K раствору, образовавшемуся при действии 89,3 мл раствора серной кислоты (массовая доля кислоты 39,2%, плотность раствора 1,4 г/мл) на 20,6 г гидроксида хрома (3) прибавили 225 г раствора сульфида бария (массовая доля соли 33,8%) и образовавшуюся смесь слегка нагрели до окончания реакций. Вычислите массовые доли веществ, содержащихся в растворе после окончания опыта.
B ответе сказано: 2,86% Cr2(SO4)3 - как это получилось?
Считаем моли:
Кислота 89,3*1,4*0,392/98=0,5M
Гидроксид хрома 20,6/103=0,2M
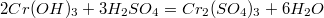
Легко сосчитать, что в результате получится раствор без кислоты, но c наличием 0,167M сульфата хрома.
Теперь, сульфид бария.
Снова считаем моли:
225*0,338/169=0,45M

Нагревали, очевидно, чтобы весь сульфат бария растворялся и реагировал.
Снова очевидная вещь: в реакцию вступит 0,15M сульфата хрома, и, не менее очевидно, что в этой жуткой смеси его останется 0,017M или 0,017*392=6,664 г.
Сосчитаем массу всей смеси. Газов у нас не выделялось, поэтому тупо складываем:
89,3*1,4+20,6+225=370,62 г.
Ну, и массовая доля сульфата хрома:
6,664*100%/370,62=1.79%
Единственный способ получить ответ из задачника - нафантазировать образование жуткого комплекса
_3$$ $$[Cr_2(H_2O)_{13}](SO_4)_3$$](http://fx.ifz.ru/tex2.php?d=120&i=%24%24%5BCr_2%28H_2O%29_%7B13%7D%5D%28SO_4%29_3%24%24)
, который, судя по справочникам имеет право на существование. Ho это уже мои измышления...