Энтропия
Добавлено: 11 июн 2014, 05:43
Термодинамический смысл:

Но он спрашивает, а чему собственно равна энтропия.
Я не понимаю, то ли мне нужно было сказать про статистический смысл энтропии
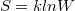
или, что это функция аддитивна. Или что-то другое?
Спасибо)
Но он спрашивает, а чему собственно равна энтропия.
Я не понимаю, то ли мне нужно было сказать про статистический смысл энтропии
или, что это функция аддитивна. Или что-то другое?
Спасибо)