Почему так? dU+pdV = dH, а dH = TdS в состояния равновесия, которое к этому не имеет никакого отношения...?
Найдено 52 соответствий
- 28 май 2011, 19:10
- Форум: Для начинающих
- Тема: Что там под кривой?
- Ответов: 21
- Просмотров: 263
Что там под кривой?
Почему так? dU+pdV = dH, а dH = TdS в состояния равновесия, которое к этому не имеет никакого отношения...?
- 28 май 2011, 17:52
- Форум: Для начинающих
- Тема: Что там под кривой?
- Ответов: 21
- Просмотров: 263
Что там под кривой?
Мне не видно... :search: размерность теплоёмкости Дж/(моль*К) если ещё разделить на температуру то будет Дж/(моль*К^2) а такой энтропии не бывает...
- 28 май 2011, 17:30
- Форум: Для начинающих
- Тема: Что там под кривой?
- Ответов: 21
- Просмотров: 263
Что там под кривой?
При изменении температуры от Т1 до Т2 изменится внутреняя энергия системы, равная грубо говоря изменению энтальпии. Далее  а в формуле наоборот c_p / T :blink: как это?
а в формуле наоборот c_p / T :blink: как это?
- 28 май 2011, 16:57
- Форум: Для начинающих
- Тема: Что там под кривой?
- Ответов: 21
- Просмотров: 263
Что там под кривой?
Ладно, спрошу по другому... Формула расчета изменения энтропии от температуры:  почему изменение энтропии от T1 до T2 равно теплоемкость/температуру? и на какую температуру, если она меняется от T1 до T2 ???
почему изменение энтропии от T1 до T2 равно теплоемкость/температуру? и на какую температуру, если она меняется от T1 до T2 ???
- 28 май 2011, 11:32
- Форум: Для начинающих
- Тема: Что там под кривой?
- Ответов: 21
- Просмотров: 263
Что там под кривой?
Возьмем график функции роста энтропии в дали от фазовых переходов, т.е. по оси абсцисс будет температура а по оси ординат - энтропия (функция S(T)). Тогда чему будет равна площадь под кривой, ограниченной температурами T2 и T2, т.е. интеграл 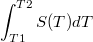 ?
?
- 28 май 2011, 10:29
- Форум: Физика
- Тема: Сложная задача на теплоемкость
- Ответов: 12
- Просмотров: 98
Сложная задача на теплоемкость
Для простоты я принял, что изменение теплоёмкости вне фазового перехода отсутствует, в итоге получился четырехугольник, одна сторона которого равна приращению температуры, вторая - приращению теплоёмкости (функция c(T)) а площадь - изменению энтальпии (функции H(T)). Изменение энтальпии составило 23...
- 28 май 2011, 10:01
- Форум: Физика
- Тема: Сложная задача на теплоемкость
- Ответов: 12
- Просмотров: 98
Сложная задача на теплоемкость
Изменение энтальпии на участке 25-35*С соответствует 2444-2421 = 23 кДж/кг, значит теплоемкость уменьшится на 23/10=2,3 кДж/(кг*К) что равно 41,4 Дж/(моль*К) и станет равна 75,3 - 41,4 = 39,9 Дж/(моль*К). Соответствует ли эта цифра реальной теплоёмкости водяного пара при температуре 30*С ?
- 27 май 2011, 14:47
- Форум: Физика
- Тема: Сложная задача на теплоемкость
- Ответов: 12
- Просмотров: 98
Сложная задача на теплоемкость
Энтальпия пара H'' определяется через известные по условию энтальпию жидкости Н' (известна не энтальпия, а теплоемкость, но этого достаточно)
Что то я не пойму как зная только одну теплоёмкость можно определить абсолютное значение энтальпии?
- 27 май 2011, 04:32
- Форум: Физика
- Тема: Сложная задача на теплоемкость
- Ответов: 12
- Просмотров: 98
Сложная задача на теплоемкость
Вы про эту формулу что ли  ? Но для нее нужно будет брать из справочника данные энтальпии водяного пара и испарения... или на это задача и расчитана?
? Но для нее нужно будет брать из справочника данные энтальпии водяного пара и испарения... или на это задача и расчитана?
- 26 май 2011, 11:24
- Форум: Физика
- Тема: Сложная задача на теплоемкость
- Ответов: 12
- Просмотров: 98
Сложная задача на теплоемкость
Теплота испарения воды при 35 *С равна 2421 кДж/кг а при 25 *С = 2444 кДж/кг. Оцените среднее значение изобарной теплоемкости водяного пара в интервале температур 25 - 35 *С, если c_p(H2O(ж)) = 75,3 Дж/(моль*К). Даже не могу придумать, как её решить... ведь при фазовом переходе жидкость -> газ тепл...